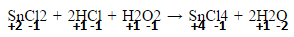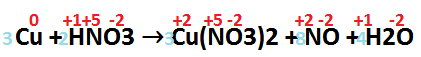Confira questões resolvidas sobre as Reações de Oxirredução:
1) ENEM 2014 – A aplicação excessiva de fertilizantes nitrogenados na agricultura pode acarretar alterações no solo e na água pelo acúmulo de compostos nitrogenados, principalmente a forma mais oxidada, favorecendo a proliferação de algas e plantas aquáticas e alterando o ciclo do nitrogênio, representado no esquema. A espécie nitrogenada mais oxidada tem sua quantidade controlada por ação de microrganismos que promovem a reação de redução dessa espécie, no processo denominado desnitrificação.
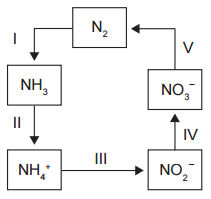
O processo citado está representado na etapa
A) I.
B) II.
C) III.
D) IV.
E) V.
2) (Cesgranrio) – Observe a reação: SnCl2 + 2HCl + H2O2 → SnCl4 + 2H2O. A partir dela, podemos afirmar corretamente que o:
a) Sn e o Cl sofrem oxidação.
b) Sn sofre oxidação, e o O, redução.
c) Sn sofre oxidação, e o HCl, redução.
d) H2O2 sofre redução, e o Cl, oxidação.
e) H2O2 sofre oxidação, e o Sn, redução.
3) ITA SP – Na equação iônica: Ni + Cu++(aquoso) ——-> Ni++(aquoso) + Cu:
a) o níquel é o oxidante porque ele é oxidado.
b) níquel é o redutor porque ele é oxidado.
c) o íon cúprico é oxidante porque ele é oxidado.
d) o íon cúprico é o redutor porque ele é reduzido.
e) Não há oxidante nem redutor, pois não se trata de uma reação de óxido-redução)
4) (UFMS/2008) – O cobre metálico sofre oxidação na presença de ácido nítrico, de acordo com a equação não balanceada: Cu + HNO3 → Cu(NO3)2 + NO + H2O . A respeito dessa reação, é correto afirmar:
01. O cobre recebe dois elétrons.
02. O nitrogênio é o agente oxidante.
04. O nitrogênio sofre oxidação.
08. O cobre é o agente redutor.
16. A soma dos coeficientes dos reagentes e produtos da equação é igual a 20.
5) (FUVEST-SP) – Considere as seguintes reações químicas:
I- SO2 + H2O2 → H2SO4
II- SO2 + H2O → H2SO3
III- K2Cr2O7 + HBr → KBr + CrBr3 + Br2 + H2O
Pode-se classificar como reação de oxirredução, apenas:
a) I
b) II
c) III
d) I e III
e ) II e III
6) ITA – Esta questão refere-se a uma experiência em que um professor mostrou a dissolução completa do cádmio metálico pelo ácido clorídrico realizada num béquer. Ele chamou a atenção para os aspectos notáveis dessa dissolução, tais como: aquecimento espontâneo do béquer, desprendimento gasoso durante a solução, formação final de apenas uma solução incolor. E perguntou:
I. O cádmio sofre oxidação?
II. A reação exotérmica?
III. O cloreto de cádmio é solúvel em água?
IV. O gás desprendido é cloro?
Para qual (ou quais) das perguntas, a(s) resposta(s) é(são) afirmativa(s)?
a) Somente para as perguntas I, II, III.
b) Somente para as perguntas II e IV.
c) Somente para as perguntas I e III.
d) Somente para as perguntas IV.
e) Para todas as perguntas.
7) (Pucmg) – Sobre a equação de oxi-redução:
Cr2O3 + Al ——–> Al2O3 + Cr
É CORRETO afirmar que:
a) o cromo do Cr2O3 sofre redução na reação.
b) o óxido de cromo III funciona como o redutor da reação.
c) o oxigênio sofre oxidação na reação.
d) o alumínio funciona como o oxidante da reação.
e) após o balanceamento da equação, a soma dos coeficientes mínimos e inteiros das espécies químicas envolvidas é igual a 4.
8) (UFRGS) – O agente ativo dos alvejantes de uso doméstico é o íon hipoclorito, ClO-. Nos processos de branqueamento, esse íon sofre redução; isso significa que
a) a substância que sofre a ação do hipoclorito recebe elétrons.
b) ocorre diminuição do número de elétrons na sua estrutura.
c) ClO- é agente redutor.
d) ClO- é convertido em cloro elementar ou íon cloreto.
e) não ocorre transferência de elétrons.
9) (UFRGS) – Entre os processos abaixo, o que NÃO envolve reações de oxirredução é o de
a) neutralização de um ácido.
b) produção de eletricidade numa célula eletroquímica.
c) corrosão de uma barra metálica.
d) formação de ferrugem numa esponja de aço.
e) recuperação de prata de radiografias usadas.
10) ITA – Qual das afirmações abaixo é FALSA em relação a reações de oxido-redução?
a) O número de elétrons perdidos pelos átomos “redutores” é igual ao número de elétrons ganhos pelos átomos “oxidantes”.
b) O oxidante se reduz e o redutor se oxida.
c) Um bom oxidante é também um bom redutor.
d) Na eletrólise, num eletrodo ocorre uma redução enquanto que no outro se processa uma oxidação.
e) Um bom oxidante depois de reduzido torna-se um mau redutor.
11) UFRGS – Por efeito de descargas elétricas, o ozônio pode ser formado na atmosfera. a partir da sequencia de reações representadas a seguir:
I. N2 + O2 → 2 NO
II. 2 NO + O2 → 2 NO2
III. NO2 + O2 → NO + O3
considerando as reações no sentido direto, pode-se afirmar que ocorre oxidação do nitrogênio:
a) apenas em I.
b) apenas em II
c) apenas em I e II
d) apenas em I e III
e) em I, II e III
19
Visitas totales
19
Visitantes únicos