Confira questões resolvidas sobre o Equilíbrio Iônico:
1) ENEM 2015 – Vários ácidos são utilizados em indústrias que descartam seus efluentes nos corpos d’água, como rios e lagos, podendo afetar o equilíbrio ambiental. Para neutralizar a acidez, o sal carbonato de cálcio pode ser adicionado ao efluente, em quantidades apropriadas, pois produz bicarbonato, que neutraliza a água. As equações envolvidas no processo são apresentadas:
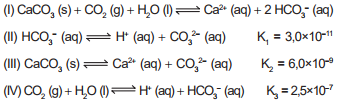
Com base nos valores das constantes de equilíbrio das reações II, III e IV a 25 °C, qual é o valor numérico da constante de equilíbrio da reação I?
A) 4,5×10^-26
B) 5,0×10^-5
C) 0,8×10^-9
D) 0,2×10^5
E) 2,2×10^26
2) ITA 2009 – Sabendo que a constante de dissociação do hidróxido de amônio e a do ácido cianídrico em água são, respectivamente, Kb =1,76 x 10–5 (pKb = 4,75) e Ka = 6,20 x l0–10 (pKa = 9,21), determine a constante de hidrólise e o valor do pH de uma solução aquosa 0,1 mol L–1 de cianeto de amônio.
3) (UESPI) – A fadiga muscular, comum quando se executa um grande esforço físico, é causada pelo acúmulo do Ácido Láctico (HC3H5O3) nas fibras musculares de nosso organismo. Considerando que, em uma solução aquosa 0,100M, temos 3,7% do ácido láctico dissociado, determine o valor da constante de acidez (Ka).
Dados de massa atômica: H=1; O=16; C=12.
a) 1,0 x 10–1
b) 1,4 x 10–4
c) 2,7 x 10–2
d) 3,7 x 10–2
e) 3,7 x 10–3
4) (SANTA CASA) – A 45°C o produto iônico da água é igual a 4 x 10-14. A essa temperatura o valor de [H+] de uma solução aquosa neutra é:
a) 6 x 10-7
b) 2 x 10-7
c) 4 x 10-7
d) 2 x 10-14
e) 4 x 10-14
5) (PUC) – Para conseguirmos aumentar o pH de uma solução aquosa, devemos nela borbulhar o gás:
a) clorídrico
b) amônia
c) cianídrico
d) carbônico
e) hidrogênio
6) (UFSM-RS) – Considere as constantes de ionização dos ácidos I, II e III: KI = 7,0 · 10–5 ; KII = 1,0 · 10–7 ; KIII = 2,0 · 10–9. Colocando-os em ordem crescente de acidez, têm-se:
a) I, II e III.
b) I, III e II.
c) II, III e I.
d) III, I e II.
e) III, II e I.
7) (UFMG) – Considere certa quantidade de água e suco de limão, misturados, contida em um copo. Analise estas três afirmativas concernentes a esse sistema:
I. O sistema é ácido.
II. O pH do sistema é maior que 7.
III. No sistema, a concentração dos íons H+ é maior que a dos OH–.
A partir dessa análise, é CORRETO afirmar que
A) apenas as afirmativas I e II estão certas.
B) apenas as afirmativas I e III estão certas.
C) apenas as afirmativas II e III estão certas.
D) as três afirmativas estão certas.
8) (UFRS) – Tem-se duas soluções aquosas:
I – solução de NaOH 0,01 mol/L
II – solução de HCl 0,01 mol/L
O quociente pH da solução I/pH da solução II é igual a:
a) 1.
b) 6.
c) 10.
d) 10^-2
e) 10^-10
9) (E. E. Mauá-SP) – Uma solução 1 M de ácido benzoico tem o mesmo pH que outra solução aquosa de cloreto de hidrogênio de concentração 8,0 · 10–3 mol/L. Dado: log 2 = 0,3
a) Calcule o pH da solução de ácido clorídrico.
b) Qual o grau de ionização do ácido benzoico?
c) Calcule a constante de ionização do ácido benzoico.
a) Calcule o pH da solução de ácido clorídrico.
b) Qual o grau de ionização do ácido benzoico?
c) Calcule a constante de ionização do ácido benzoico.
10) (PUC-MG) – Ao analisar um determinado suco de tomate, um técnico determinou que sua concentração hidrogeniônica é igual a 0,001 mol/L. Assim, o pH desse suco de tomate é:
a) 2
b) 3
c) 4
d) 9
e) 11
16
Visitas totales
14
Visitantes únicos
